Az izotópok rokoni viszonyai
A kb. 120 kémiai elemnek kb. 3500 atommagfajtája (nuklidja, izotópja) ismert. Azért nincsenek határozott számok, mert a méréstechnika fejlődésével egyre rövidebb élettartamú (gyorsan bomló) atommagok kimutatása, vizsgálata válik lehetségessé, így a fenti szám folyamatosan növekszenek. Ebből a több ezer izotópból azonban csupán 254 stabil (azaz "végtelen" hosszú felezési idejű), tehát az izotópok nagy többsége radioaktív. Ezért egy radioaktív bomlás eredményeképp a létrejövő "leánymag" nagy valószínűséggel szintén radioaktív lesz, azaz újabb radioaktív bomlás fog következni. Sőt, az is lehet, hogy az egymást követő bomlások sok-sok lépésen keresztül radioakív anyagokhoz vezetnek, ilyenkor bomlási sorról beszélünk. Tehát csupán egyetlen radioaktív izotópból kiindulva is sok különböző radioaktív leánymag születhet meg sponttán módon, létrehozva ezzel a saját "családját" a több ezer izotóp tengerében.
A radioaktív izotópok mindegyike "alapíthat családot", és mivel kb. 3500-an vannak, elsőre úgy tűnhet, hogy itt egy rengeteg családból álló, bonyolult rokonsági rendszer van. De az is igaz, hogy nem tud minden izotóp saját famíliát alapítani, hiszen sokuk már egy radioaktív bomlás eredményeként születik meg, vagyis már benne vannak egy családban. Ez alapján hogyan képzelhetjük el az izotópok családfáját?
A számelmélet besegít
Nézzük meg, hogy a radioaktív bomlásoknak 3 fajtájában hogyan változik az elbomló mag $A$ tömegszáma!
Bomlási | Tömegszám- |
| alfa- | $\Delta A=-4$ |
| béta- | $\Delta A=0$ |
| gamma- | $\Delta A=0$ |
Tehát a tömegszám az alfa-bomlásban mindig 4-gyel csökkena, béta- és a gamma-bomlásban pedig nem változik. Ezért egy atommag akármilyen fajtájú radioaktív bomlások sokaságát szenvedi is el (akárhány lépésben), a folyamatban létrejövő összes atommag olyan lesz, hogy a tömegszámaik 4-gyel osztva ugyanannyi maradékot fognak adni.
Hányféle maradék lehetséges 4-gyel való osztáskor? Négyféle: 0; 1; 2; vagy 3. Ezért a radioaktív izotópok a tömegszámaik alapján 4 csoportba, "családba" rendezhetők.
4-gyel | Az ilyen | A tömegszám | Bomlási család |
| \(0\) | \(4n\) | \(A=4n\) | tórium |
| \(1\) | \(4n+1\) | \(A=4n+1\) | neptúnium |
| \(2\) | \(4n+2\) | \(A=4n+2\) | urán-rádium |
| \(3\) | \(4n+3\) | \(A=4n+3\) | aktínium |
Radioaktív bomlás révén tehát "lehetetlen kilépni a családból". A radioaktív bomlási családok tagjai között a hasonlóságot nem a közös gének jelentik, hanem hogy a tömegszámaikat 4-gyel osztva ugyanakkora maradékot produkálnak. Itt kasztrendszer van: amelyik családba születtél, biztosan annak taja lesz minden leszármazottad, akárhány generáció telik is el. Tehát egy olyan radioaktív mintában, ami kezdetben monoizotópos, csak a kezdeti izotóp családjának tagjai jöhetnek létre később, akárhogy is zajlanak benne a bomlások (tetszőleges fajtájúak, tetszőleges sorrendben).
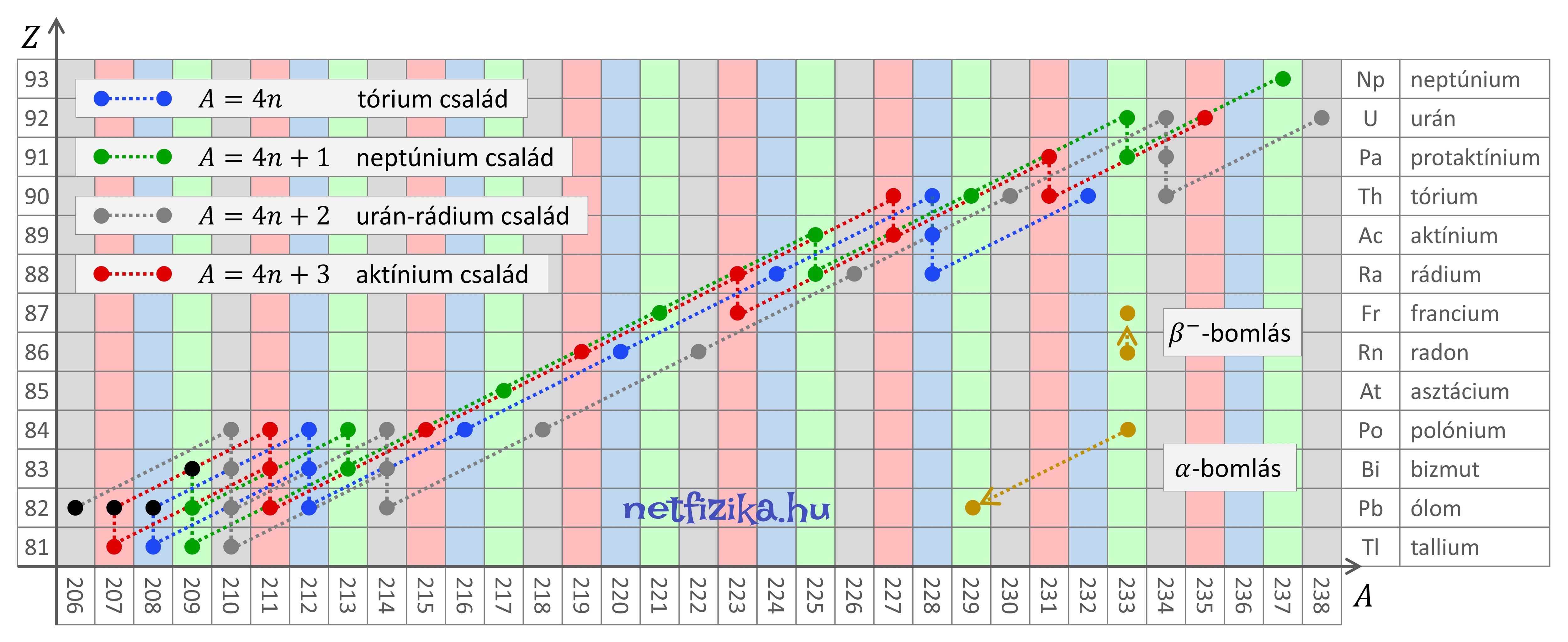
A bomlási sorokat (családokat) szokás ábrázolni derékszögű koordinátarendszerben, melynek tengelyei például \(Z\thinspace \unicode{x2013}\thinspace A\) azaz rendszám-tömegszám. Itt a családokat azonos színű oszlopok jelenítik meg, és mivel 4 család van, 4 szín elég az ábrázoláshoz:
A bomlási sorok úgy érnek véget, hogy a keletkező izotóp már nem bomlik tovább, vagyis stabil, azaz "végtelen felezési idejű". Ezeket fekete pöttyök jelzik.
Kik találhatók meg a természetben?
A Földön a természetben nem található meg mindenféle izotóp. Ennek nemcsak az az oka, hogy a Földön a keletkezésekor sem volt mindenféle izotóp jelen, hanem mert a Föld életkora kb. 4,5 milliárd év, ami sok radioaktív izotóp számára borzasztóan hosszú idő. Még egy viszonylag hosszú, mondjuk 100 millió éves felezési idejű izotópot nézve is, a Föld születése óta.
\[\frac{4,5\cdot 10^9\ \mathrm{év}}{100\cdot 10^6\ \mathrm{év}}\approx45\]
alapján a kezdeti mennyiség már 45-ször "lefeleződött". A bomlástörvény alapján a kezdeti mennyiségből megmaradó hányad:
\[N=N_0\cdot 2^{-\frac{t}{T}}\]
\[N=N_0\cdot 2^{-\frac{45T}{T}}\]
\[N=N_0\cdot 2^{-45}\]
\[N=N_0\cdot 3\cdot 10^{-14}\]
vagyis a kezdeti magok közül minden 30 ezer milliárból csak egy maradt meg. Ezért ha egy izotóp felezési ideje 100 millió évnél rövidebb (és a Föld keletkezése óta már nem termelődött), akkor mára gyakorlatilag teljesen eltűnt. Ugyan nem húzható éles határ, hogy mekkora felezési idejű izotópok "fogytak már el lényegében teljesen" a Föld keletkezése óta, de általában ezt 100 millió évnek szokták venni.
A Földön megtalálható 339 izotóp közül 286 a Naprendszer születésekor már létezett (ezek az ún. primordiális izotópok). A 286‑ból 252 stabilnak tekinthető, a többi 34 pedig ugyan radioaktív, de legalább 100 millió év a felezési ideje, ezért "még maradt belőle". Voltak izotópok, amelyek a Naprendszer keletkezésekor létezhettek, de mára mind elbomlottak, és vannak olyanok, amelyek a Naprendszer keletkezése után jöttek létre.
A földi természetben jelenleg megtalálható radioaktív izotópok a keletkezésük szerint három csoportba sorolhatók:
- a Föld keletkezésekor volt belőle, és elég hosszú a felezési ideje (100 millió évnél nagyobb; ilyenből 34 izotóp van)
- a fenti 34 radioaktív izotóp valamelyikéből radioaktív bomlással keletkezett, illetve folyamatosan keletkezik, termelődik
- kozmikus eredetű folyamatokban termelődik (pl. kozmikus sugárzás hatására a légkörben jön létre a \(\displaystyle \mathrm{{}^{14}C}\) amit radiokarbonnak nevezünk)
R.I.P
Az \(A=4n+1\) alakú neptúnium családban a 100 millió éves "határnál" csak jóval rövidebb felezési idejű izotópok szerepelnek, ezért ennek a Föld keletkezésekor meglévő magjai azóta már mind rég elbomlottak. Más családokból pedig nem lehetséges átlépni radioaktív bomlással. Ezért ez a család mára kihalt. Úgy is fogalmazhatunk, hogy a család nem rendelkezett hosszú távra tekingető taggal (elég hosszú felezési idejű taggal), így mára felélték minden tartalékukat. Ennek a tékozló családnak a leghosszabb élettartamú izotópja, a bomlási sor elején található \(\displaystyle \mathrm{{}^{237}_{\ \ 93}Np}\) is "csak" 2,2 millió éves felezési idővel rendelkezik, vagyis a Föld születése óta már több, mint 2000 alkalommal megfeleződött, tehát mostanra a kezdeti mennyiség
\[\frac{1}{2^{2000}}\approx 8,7\cdot 10^{-603}\]
részaránya maradt csak meg. Ezt esetleg még ki lehetne mutatni? Aligha, hiszen a Földön összesen \(\displaystyle \approx 10^{50}\) atom van, úgyhogy teljesen nyugodtan mondhatjuk, hogy a Föld születésekor meglévő összes \(\displaystyle \mathrm{{}^{237}_{\ \ 93}Np}\) már mind elbomlott. Jelenlegi becsléseink szerint még az egész Univerzumban is csak \(\displaystyle \approx 10^{82}\) atom van összesen.
Mégis van élet a halál után?
A neptúnium család egészen kis mennyiségben mégis jelen van a természetben, ugyanis a kasztrendszer merev falán létezik egy picinyke kiskapu: ha egy atommagot eltalál egy neutron, és a mag azt befogja, akkor a mag tömegszáma 1-gyel növekszik, vagyis a 4-gyel osztási maradéka mégiscsak megváltozik. De honnan jöhetne egy neutron? Erre több lehetőség is van:
- Spontán hasadások révén: a földkéregben lévő \(\displaystyle \mathrm{{}^{235}U}\) és a \(\displaystyle \mathrm{{}^{238}U}\) izotópok nem mindig alfa-bomlással alakulnak át (700 millió illetve 4,5 milliárd év felezési idővel), hanem néha spontán hasadással bomlanak el (átlagosan 5 millió illetve 20 ezer uránmagra jut egy ilyen folyamat). Ilyenkor a közepes méretű leánymagok mellett néhány szabad neutron is keletkezik (átlagosan 1,86 illetve 2,07).
- $(\alpha;\ n)$ reakcióban: egy alfa-bomlásban keletkezett alfa-részecske amikor eltalál egy atommagot, néha nem egyszerűen elnyelődik benne, hanem a végén egy neutron kilökődik az eltalált magból
- $(\gamma;\ n)$ reakcióban: ilyenkor egy gamma-foton kiüt egy neutront az eltalált atommagból
Akárhogy is keletkezett egy neutron, ő elnyelődve egy atommagban átjárást biztosít a bomlási családok között. A neptúnium-sor kezdő tagja, a \(\displaystyle \mathrm{{}^{237}Np}\) a természetben található két uránizotópból jön létre, kétféle módon. Vagy egy ${}^{235}_{92}\mathrm{U}$ mag nyel el két neutron, majd béta-bomlást szenved:
$${}^{235}_{92}\mathrm{U}+{}^1_0\mathrm{n} \to {}^{236}_{92}\mathrm{U}+\gamma$$
$${}^{236}_{92}\mathrm{U}+{}^1_0\mathrm{n} \to {}^{237}_{92}\mathrm{U}+\gamma$$
$${}^{237}_{92}\mathrm{U} \xrightarrow{\beta ^-}{}^{237}_{93}\mathrm{Np}+\mathrm{e^-}+\overline{\nu}_{\mathrm{e}}$$
vagy egy ${}^{238}_{92}\mathrm{U}$ magból egy neutron "kiüt" még egy neutront, majd béta-bomlást szenved:
$${}^{238}_{92}\mathrm{U}+{}^1_0\mathrm{n} \to {}^{237}_{92}\mathrm{U}+2{}^1_0\mathrm{n}$$
$${}^{237}_{92}\mathrm{U} \xrightarrow{\beta ^-} {}^{237}_{93}\mathrm{Np}+\mathrm{e^-}+\overline{\nu}_{\mathrm{e}}$$
A spontán hasadásokról itt találhatók továbbiak.
A máig élő családok
A másik 3 bomlási sor máig megtalálható a természetben, mert ezek elején a Föld korával összemérhető felezési idejű izotópok találhatók, amik még most is folyamatosan "ontják magukból a leánymagokat", azaz megállás nélkül "szülik" a családjuk tagjait:
| Bomlási család | Leghosszabb élettartamú izotóp | ||
| jele | felezési ideje | ||
| jele | neve | ||
| \(4n\) | tórium | \(\displaystyle \mathrm{{}^{232}_{\ \ 90}Th}\) | 14 milliárd év |
| \(4n+1\) | neptúnium | \(\displaystyle \mathrm{{}^{237}_{\ \ 93}Np}\) | 2,2 millió év |
| \(4n+2\) | urán-rádium | \(\displaystyle \mathrm{{}^{238}_{\ \ 92}U}\) | 4,5 milliárd év |
| \(4n+3\) | aktínium | \(\displaystyle \mathrm{{}^{235}_{\ \ 92}U}\) | 700 millió év |
A radioaktív bomlási sorok "izotóptermelésének" egyik érdekes, az ókori történelmet a modern fizikával egybehozó története itt olvasható.
Miért "logikátlan" két család neve?
Az aktínium-sorozatot azért így hívják, mert a lánc elkülönítésekor még nem tudták, hogy a \(\displaystyle \mathrm{{}^{227}Ac}\) aktínium nem a sor eleje, hanem ő egy természetben máig meglévő izotópnak, az \(\displaystyle \mathrm{{}^{235}U}\) uránnak a bomlási terméke. Ugyanígy az urán-rádium sorozatnál kezdetben úgy gondolták, hogy a rádium a kiinduló anyag, és csak később derült ki, hogy ott a \(\displaystyle \mathrm{{}^{238}U}\) urán indítja a bomlási sort (ő termeli folyamatosan a \(\displaystyle \mathrm{{}^{226}Ra}\) rádiumot).